
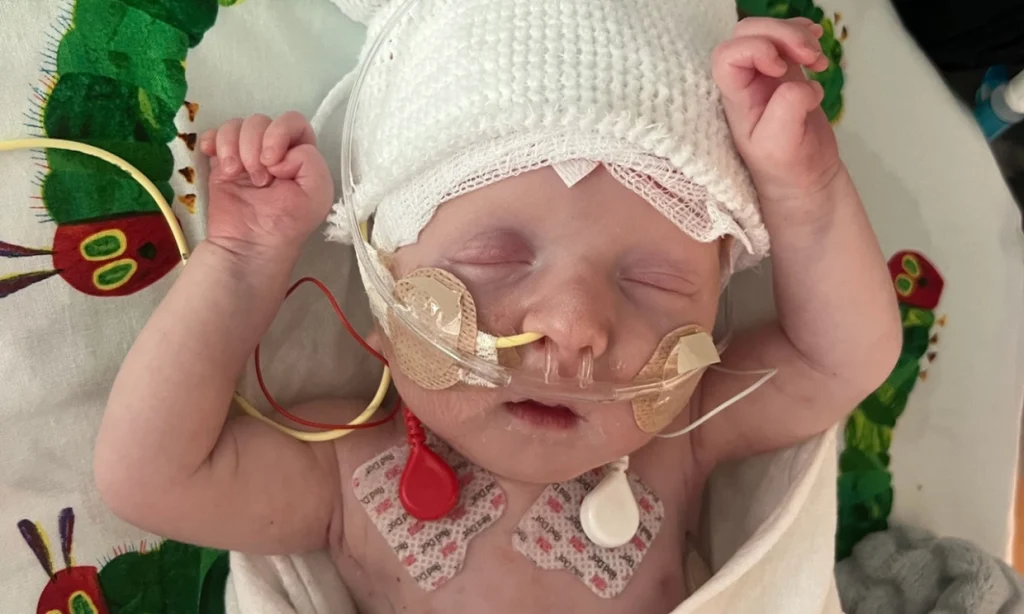
برای نخستین بار در جهان، دیانای یک نوزاد برای درمان بیماری ژنتیکی کشندهای که به آن مبتلا بود، توسط پزشکان بازنویسی شد. کِیجی مولدون کوچولو که اکنون ۱۵ ماهه است، تنها چند روز پس از تولد به بیماری بسیار نادری مبتلا شد؛ از جمله علائم کِیجی مولدون میتوان به بیحالی شدید و مشکلات تنفسی اشاره کرد.
آزمایشها مشخص کرد که سطح آمونیاک در خون او بهشدت افزایش یافته بود. این بیماری که کاهش عملکرد CPS1 نام دارد، باعث میشود کبد او نتواند آمونیاک را به درستی دفع کند. تجمع آمونیاک در بدن میتواند به آسیب دائمی مغز یا حتی مرگ منجر شود. در صورت عدم درمان این تجمع آمونیاک در بدن، احتمال مرگ نوزاد در عرض چند روز وجود داشت.
نیکول، مادر کیجی، در ویدیویی که توسط بیمارستان کودکان فیلادلفیا (CHOP) منتشر شده میگوید: «وقتی در گوگل عبارت کاهش عملکرد CPS1 را جستوجو میکنی، یا با آمار مرگ و میر ناشی از آن و یا با پیوند کبد مواجه میشوی… ما کاملاً شوکه شده بودیم».
طبق مقالهای که در مجله پزشکی نیوانگلند منتشر و توسط دانشمندانی نوشته شده که درمان کیجی را انجام دادند، کمبود CPS1 جزو یکی از شدیدترین و نادرترین اختلالات چرخه اوره به شمار میرود. این بیماری تقریباً از هر ۸۰۰ هزار تا ۱.۳ میلیون تولد، یک نفر را درگیر خودش میکند. زمانی که بیماری کیجی تشخیص داده شد، تنها راه درمان آن، پیوند کبد بود که بیشتر برای کودکان بزرگتر و سالمتر مناسب است، نه برای کیجی که وضعیت سلامتیاش بسیار ضعیف بود.
نیکول در این باره میگوید: «با اینکه کوچیک بود، ولی خیلی مقاومت میکرد». کایل، پدر این نوزاد کوچولو، هم اضافه میکند: «او از همان ابتدا یک مبارز واقعی بود».
گوجهفرنگی بنفش اصلاح ژنتیکی شده که سالمتر از گوجهفرنگی قرمز است

کیجی را زیر دستگاه دیالیز گذاشتند تا آمونیاک خونش کاهش پیدا کند؛ به این ترتیب او در بیمارستان ماند تا وقتی به اندازه کافی بزرگ شد، برای او پیوند کبد انجام دهند. اما وقتی که تنها شش ماه داشت، پزشکان برای اولین بار نخستین دوز دارو پیشرفته و نوین ویرایش ژن را به او دادند که در واقع دیانایاش را بازنویسی میکرد.
تیمی از دانشمندان بیمارستان کودکان فیلادلفیا و دانشگاه پنسیلوانیا (Penn) پیشتر روی روش استفاده از ویرایش ژن جهت ساخت درمانهای شخصیسازیشده برای بیماریهایی مثل نقص CPS1 تحقیق میکردند؛ کیران موسونورو، متخصص قلب، ژنتیک و ویرایشگر ژن در دانشگاه پنسیلوانیا و رهبر این گروه میگوید: «حدود دو سال است که روی توسعه درمانهای شخصی مشابه کار میکنیم و امیدواریم روزی برسد که بتوانیم به سرعت راهی برای اصلاح ژن معیوب هر بیمار که باعث بیماریاش شده پیدا کنیم».
ربکا آرنز-نیکلاس، متخصص ژنتیک کودکان و مدیر بیمارستان کودکان فیلادلفیا که رهبری این تحقیق را بر عهده داشت، درباره پیشنهاد این درمان به والدین کیجی میگوید: «در این بین، بزرگترین نگرانی من این بود که به یک خانواده امید کاذب بدهم… اما به نقطهای رسیدیم که فکر کردیم شاید واقعاً یک تیم بالینی و تیم توسعه دارو وجود داشته باشد که بتواند، دارویی مخصوص کیجی طراحی کند».

بعد از شش ماه تلاش، تیم دانشمندان دارویی اختصاصی برای کیجی ساختند تا جهش ژنتیکی عامل بیماری نادر او را اصلاح کند. دکتر آرنز-نیکلاس میگوید: «این دارو فقط برای کیجی طراحی شده، چون واریانتهای ژنتیکی که او دارد، خاص خودش هستند. این یعنی داروی شخصیسازیشده». در فوریه ۲۰۲۵، داروی شخصیسازیشده به داخل جریان خون کیجی تزریق شد که با استفاده از یک فناوری به نام کریسپر (CRISPR)، دیانای او را بازنویسی کرد. فناوری کریسپر مانند یک قیچی مولکولی عمل میکند که با استفاده از مولکولهای راهنما، توالی خاصی از دیانای داخل سلول را هدف قرار میدهد.
وقتی توالی هدف دیانای شناسایی میشود، آنزیمی دقیقاً در همان نقطه، دیانای را برش داده و یک توالی جدید دیانای را جایگزین آن میکند. دارویی که وارد خون کیجی شد، مستقیماً به کبد او رسید. در آنجا، دانشمندان مولکولهای راهنما را طوری برنامهریزی کرده بودند تا وارد هسته سلولهای کیجی شده و به محل جهش ژنتیکیای که عامل بیماری او بود بروند.
نیکول میگوید: «من ویرایش ژن را اینطور تصور میکردم که مثل نوشتن یک جمله روی کاغذ است… وقتی یک کلمه اشتباه نوشته میشود، برمیگردی و آن را اصلاح میکنی… ویرایش ژن باعث حذف ژنهای جهشیافته از دیانای او و جایگزینی آنها با ژنهای سالم و کارآمد میشود». کیجی، کمترین دوز ممکن از این درمان را دریافت کرد تا به بدنش فرصت کافی برای سازگاری و کاهش هرگونه خطر احتمالی را بدهد.
معجزه علمی

تصاویر ترسناک حیوانات در سال ۲۱۰۰ در صورت تداوم تکنیکهای دستکاری ژنتیک
تنها چند روز پس از آغاز درمان، کیجی علائم بهبودی ناشی از درمان نوین خود را نشان داد. او توانست بدون اینکه سطح آمونیاک در بدنش به شکل خطرناکی افزایش یابد، مقدار بیشتری از پروتئین را در رژیم غذاییاش استفاده کند. همین پیشرفت باعث شد پزشکان بتوانند بهتدریج دوز داروهای کاهشدهنده آمونیاک را پایین بیاورند. گونههایش دوباره گل انداخت و رشد جسمیاش بهطرز چشمگیری سرعت گرفت.
در طی دو ماه بعدی، کیجی دو نوبت دیگر از این دارو را دریافت کرد؛ البته اینبار با دوزهای بالاتر. او همچنان در بیمارستان کودکان فیلادلفیا تحت نظر پزشکان است و خوشبختانه هیچ عارضهی جانبی جدی از درمان را تاکنون از خودش بروز نداده. نیکول میگوید: «ما برای مدت زیادی دچار استرس و اضطراب بودیم، اما حالا انگار کمکم نوری در انتهای تونل دیده میشود و ما آن را میبینیم… وقتی به آن نوزاد کوچولوی یککیلو و هشتصد گرمی فکر میکنم و حالا این بچه قوی، تپل و سرزنده را میبینم، واقعاً خوشحال میشوم که تسلیم نشدیم و به او فرصت دادیم تا تواناییها و آیندهی درخشانش را به ما نشان بدهد».
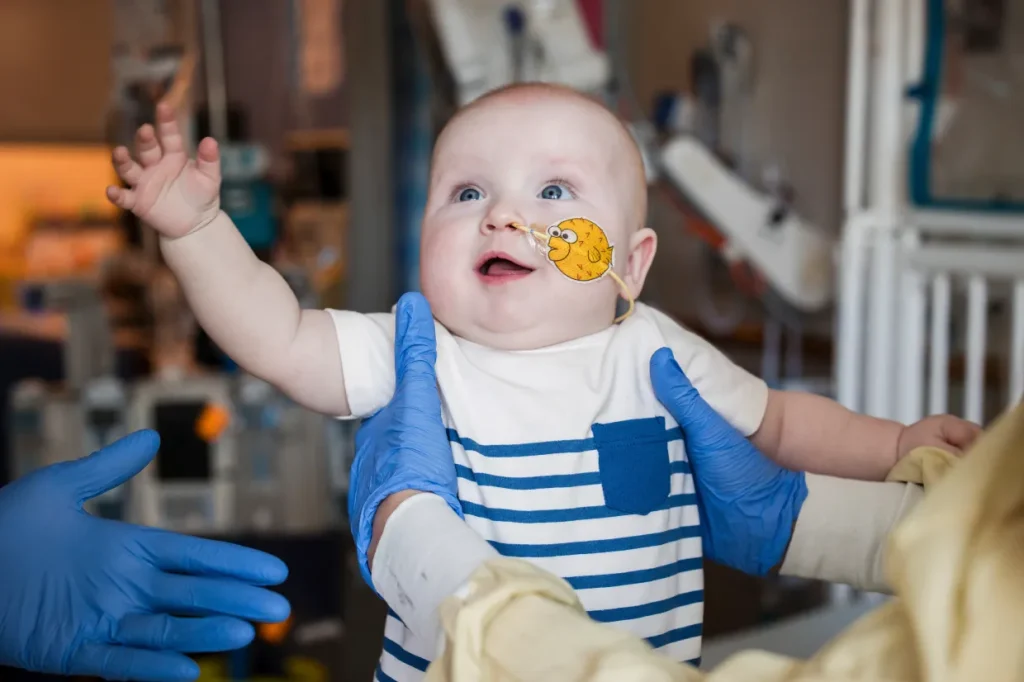
دانشمندان با احتیاط دربارهی موفقیت این روش اظهارنظر میکنند و میگویند هنوز ابعاد مختلفی در مورد وضعیت کیجی وجود دارد که تا به حال مشخص نشده — اما امیدوارند که ویرایش ژنِ شخصیسازیشده اثربخش بوده باشد. آنها تأکید کردند که باید مدت بیشتری کیجی را تحت نظر بگیرند تا بتوانند بهطور کامل مزایای این درمان را مورد ارزیابی قرار دهند. با این حال، نتایج اولیه امیدبخش است — نه فقط برای کیجی، بلکه برای سایر افرادی که به بیماریهای ژنتیکی مبتلا هستند.
این تیم پزشکی در مقاله پژوهشی خود مینویسد: «درمانهای مشابه میتوانند برای صدها نوع از بیماریهای نادر کبدی ناشی از اختلالات متابولیکی مادرزادی توسعه یابند». دکتر آرنز-نیکلاس امیدوار است که این دستاورد باعث شود کیجی در آینده با حداقل دارو — یا حتی بدون نیاز به دارو — به زندگیاش ادامه دهد. وی همچنین میگوید: «امیدواریم او آغازگر راهی باشد که بتوان آن را برای درمان دیگر بیماران، بسته به شرایط خاص هر کدام، ادامه دهیم».

پروفسور جما مارفانی، استاد ژنتیک دانشگاه بارسلونا که البته در این پژوهش نقش خاصی برعهده نداشته، میگوید: «این نخستین مورد از یک درمان کاملاً شخصیسازیشده است؛ درمانی مبتنی بر ویرایش دقیق ژن برای یک نوزاد که به یک بیماری فوقالعاده نادر و بسیار شدید مبتلا بوده… این واقعاً یک مورد بینظیر است؛ نمونهای موفق از اثبات یک ایده که در زمانی بسیار کوتاه طراحی و اجرا شده و در آن پژوهشگران و پزشکان هیچیک از مراحل پیشبالینی را نادیده نگرفتهاند… به نظر من این یک معجزه علمی است که درمان یک بیماری بسیار نادر و شدید را ممکن ساخته و دانش لازم برای درمان بسیاری از بیماریهای دیگر را فراهم میکند».
حیوانات منقرضشدهای که قرار است پس از بازگرداندن «گرگ وحشت» احیا شوند













بدون نظر